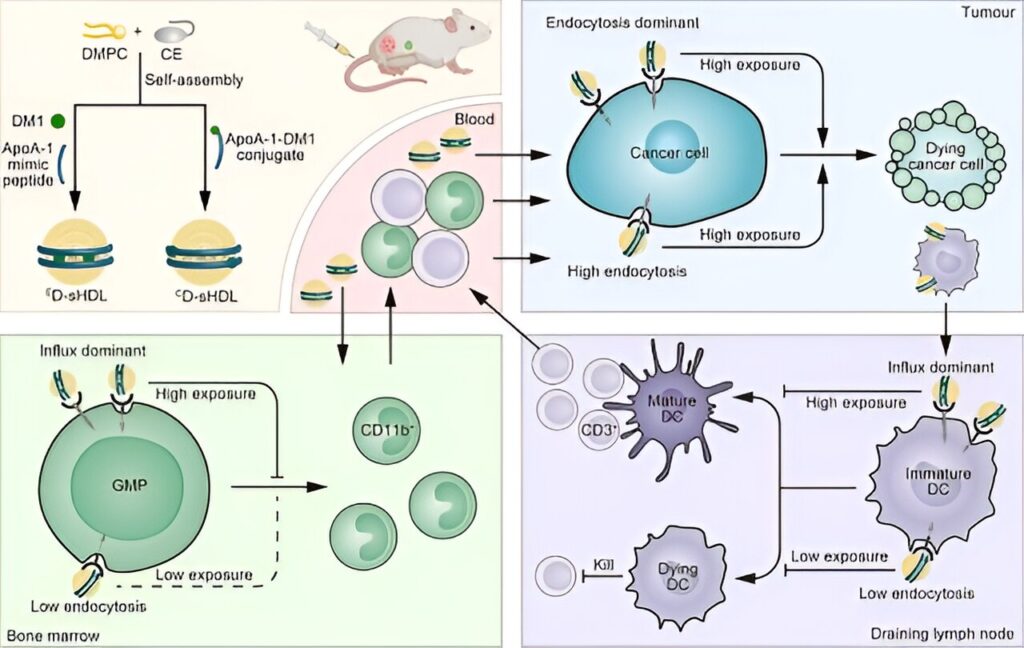
Illustration schématique de la préparation des sHDL et des différents impacts sur la toxicité et l’efficacité des schémas de chargement des médicaments dans les sHDL. Crédit : Zheng Chao
Bien que la chimiothérapie puisse stimuler l’immunité antitumorale, elle peut également altérer la fonction des cellules immunitaires et induire une lymphodéplétion, réduisant ainsi l’efficacité de l’immunothérapie ultérieure. Ainsi, des systèmes d’administration de médicaments à base de nanoparticules ont été développés pour améliorer leur biodistribution des médicaments et réduire leur toxicité, établissant ainsi un équilibre délicat entre efficacité et sécurité.
Cependant, l’interaction entre les nanoparticules et le système immunitaire, en particulier la formation de couronnes protéiques à la surface des nanoparticules, reste floue.
ApoA-1, un ligand naturel du récepteur piégeur de classe B de type 1 (SR-B1), est couramment enrichi en couronne protéique de nanoparticules lipidiques et joue un rôle crucial dans la modulation des interactions nanoparticules-cellules.
La lipoprotéine de haute densité (HDL) est une nanoparticule naturelle contenant de l’ApoA-1 et transporte principalement une cargaison hydrophobe directement dans le cytosol selon une voie indépendante de l’endocytose via la liaison avec SR-B1, tandis que l’ApoA-1 reste en circulation et subit finalement une dégradation. dans le rein.
Récemment, des HDL synthétiques (sHDL) composés de peptides mimétiques ApoA-1 ont été explorés, ressemblant aux HDL naturels en termes de biocompatibilité et de spécificité cellulaire basée sur SR-B1. Bien que d’origines différentes, les sHDL et les HDL naturels montrent tous deux la capacité de réguler les réponses immunitaires innées.
Dans une étude publiée dans Avancées scientifiquesune équipe de recherche dirigée par Zhang Pengcheng de l’Université Tech de Shanghai, Li Yaping de l’Institut de matière médicale de Shanghai de l’Académie chinoise des sciences et Wang Hao de l’Institut d’État chinois de l’industrie pharmaceutique, a révélé que l’ApoA-1 peut transporter des médicaments encapsulés dans des lipides. nanoparticules aux cellules myéloïdes, conduisant à une myélopénie et, par conséquent, à une lymphopénie, et ont démontré que ces effets secondaires peuvent être largement évités simplement en conjuguant des médicaments aux nanoparticules sans réduire l’activité antitumorale des médicaments.
Pour étudier l’influence de l’ApoA-1 sur la réponse immunitaire, les chercheurs ont créé deux variantes de lipoprotéines synthétiques de haute densité (D-sHDL) chargées de maytansine (DM1), le DM1 étant soit physiquement piégé (ED-sHDL), soit chimiquement conjugué à l’ApoA-1. 1 (CD-sHDL).
En comparant leur mécanisme d’absorption cellulaire, leur biodistribution, leur efficacité in vivo et leur sécurité, ils ont découvert que le CD-sHDL présentait une accumulation moindre dans les ganglions lymphatiques drainant la tumeur (DLN) et le fémur. Cela a entraîné une toxicité plus faible contre les cellules myéloïdes que le ED-sHDL en évitant le transport de DM1 médié par SR-B1 dans les progéniteurs granulocytes-monocytes et les cellules dendritiques.
Par conséquent, des densités plus élevées de lymphocytes dans les tumeurs, les DLN et le sang ont été enregistrées chez les souris recevant du CD-sHDL, conduisant à une meilleure efficacité et à une meilleure mémoire immunitaire contre le cancer du côlon.
De plus, les liposomes avec DM1 conjugué (CD-Lipo) ont montré une immunotoxicité plus faible que ceux avec des médicaments piégés (ED-Lipo) par le même mécanisme après l’opsonisation de l’ApoA-1 dans la protéine corona, indiquant l’universalité de l’atténuation de l’immunotoxicité par conjugaison chimique.
Compte tenu du potentiel translationnel élevé des deux nanoparticules lipidiques étudiées (sHDL et liposome) et de la prévalence de l’ApoA-1 en tant que composant principal de la couronne protéique, ces résultats éclairent la conception de stratégies de chimiothérapie basées sur les nanoparticules en élucidant le rôle de l’ApoA-1 dans moduler les réponses immunitaires.
Cette étude approfondit la compréhension de l’interaction immunitaire des nanoparticules. Comprendre l’interaction complexe entre les nanoparticules et le système immunitaire ouvrira la voie au développement de thérapies anticancéreuses plus efficaces et moins toxiques, et aura un impact sur la traduction clinique des nanoparticules pour la manipulation immunitaire.
Plus d’information:
Chao Zheng et al, La conjugaison chimique atténue l’immunotoxicité de la chimiothérapie en réduisant les fuites de médicaments médiées par les récepteurs à partir de nanoparticules lipidiques, Progrès scientifiques (2024). DOI: 10.1126/sciadv.adk9996
Fourni par l’Académie chinoise des sciences
Citation: La conjugaison chimique atténue l’immunotoxicité de la chimiothérapie des nanoparticules lipidiques (28 juin 2024) récupéré le 28 juin 2024 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni à titre d’information uniquement.