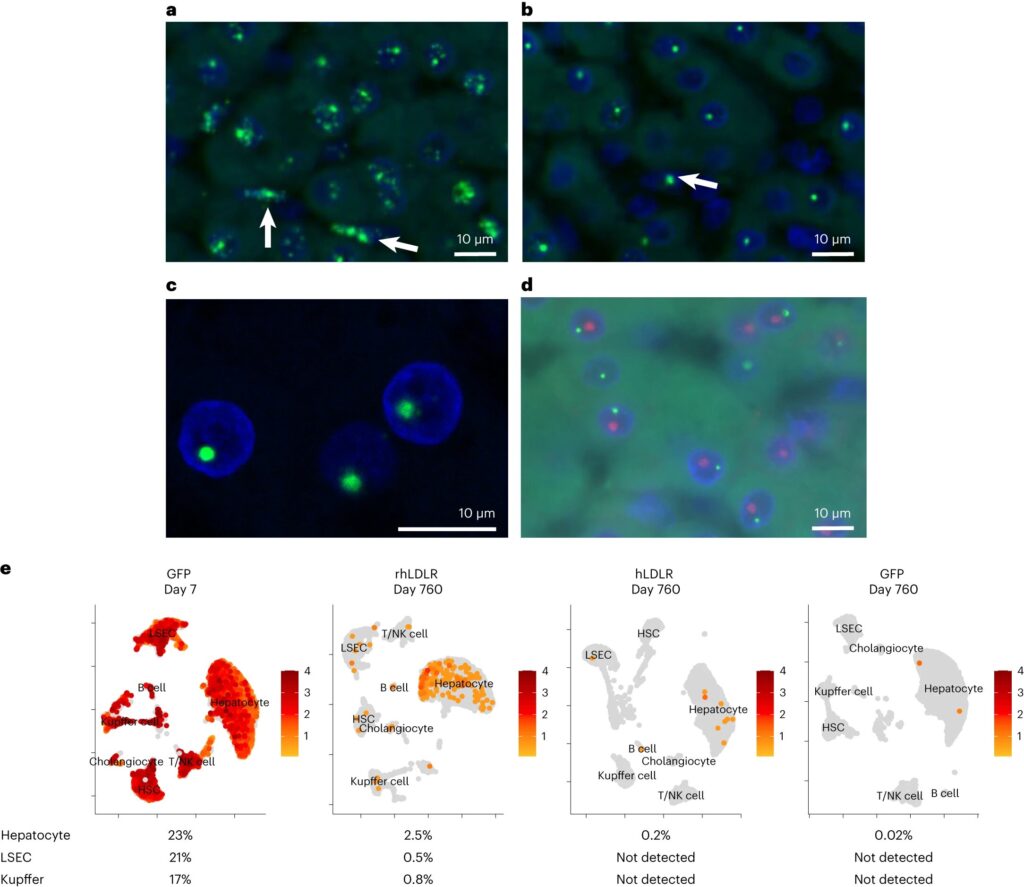
Type de cellule et absence d’association de sous-structures d’ADN et d’ARN vectoriels après l’administration iv de vecteurs AAV à des PSN. un-eles PSN ont reçu des injections iv de 1013 copies du génome par kg (poids corporel) de vecteurs AAV8 codant pour rhLDLR, hLDLR ou GFP (n = 2 par groupe). Le tissu hépatique a été collecté lors d’une biopsie hépatique (14 jours après l’administration du vecteur) ou d’une autopsie (760 jours après l’administration du vecteur). L’ISH a été réalisée sur des échantillons de foie à l’aide d’une sonde spécifique à l’ADN (liaison au brin antisens). un,bimages d’ADN ISH provenant de PSN ayant reçu du rhLDLR au jour 14 (un) et 760 (b) après l’administration du vecteur. Les flèches marquent les cellules avec un signal ADN ISH qui ne sont pas des hépatocytes ; vert, ADN vecteur ; bleu, DAPI (contre-coloration nucléaire). c,dLes sondes hybridées ont été imagées avec un microscope confocal (c) et co-coloré avec un marqueur nucléole (anticorps fibrillarine) représenté en rouge (d). e, Les noyaux ont été extraits d’échantillons d’autopsie (jour 760) et des bibliothèques d’ADNc ont été créées à partir de noyaux uniques. Les noyaux de types de cellules similaires se regroupent et le pourcentage total de noyaux exprimant l’ARN transgénique a été évalué. Pour permettre l’analyse de la transduction à un stade précoce, nous avons utilisé des échantillons provenant de deux animaux supplémentaires préalablement traités avec 7,5 × 1012 copies du génome par kg (poids corporel) de AAV8.TBG.GFP et autopsiées au jour 7 (réf. 17). Une approximation et projection de variété uniforme représentative (UMAP) est présentée pour chaque groupe ; Cellule NK, cellule tueuse naturelle ; HSC, cellule étoilée hépatique. Crédit: Biotechnologie naturelle (2023). DOI:10.1038/s41587-023-01974-7
Selon une nouvelle étude de l’Université, il est peu probable que les virus adéno-associés (AAV) de thérapie génique (virus qui peuvent être modifiés pour délivrer de l’ADN aux cellules cibles) provoquent des insertions déclenchant le cancer chez l’homme ou le singe et pourraient contribuer à son efficacité à long terme. du programme de thérapie génique (GTP) de Pennsylvanie.
Les AAV utilisés pour administrer des thérapies géniques finissent parfois par être insérés dans l’ADN chromosomique, ce qui fait craindre que de telles insertions pourraient perturber le génome de l’hôte, provoquant potentiellement un dysfonctionnement cellulaire ou le développement d’un cancer.
Cependant, deux grandes études complémentaires chez des primates non humains indiquent que les intégrations de vecteurs dans le foie des primates après une thérapie génique AAV peuvent constituer un mécanisme important pour obtenir une expression durable et sont peu susceptibles d’induire des mutations cancéreuses chez l’homme, ce qui correspond aux modèles d’intégration à faible risque observés dans infections naturelles non pathogènes à AAV.
Les thérapies géniques virales sont étudiées depuis plusieurs décennies, huit d’entre elles ayant été approuvées par la Food and Drug Administration des États-Unis pour des affections telles que l’hémophilie et la dystrophie musculaire.
La plupart utilisent des AAV pour transmettre leurs charges génétiques. Les deux nouvelles études, toutes deux publiées aujourd’hui dans Biotechnologie naturelleet Thérapie génique humaine constituent à ce jour l’exploration la plus complète des intégrations chromosomiques de l’AAV chez les primates et ont des implications importantes sur le profil de sécurité et l’efficacité à long terme des thérapies géniques basées sur l’AAV.
Les virus ont évolué pour pénétrer dans les cellules, et les chercheurs en thérapie génique les considèrent depuis longtemps comme des transporteurs ou des « vecteurs » incontournables pour les transgènes thérapeutiques. Les AAV sont les vecteurs viraux les plus couramment utilisés pour les thérapies géniques, car ils peuvent pénétrer dans les cellules en division ou non, ne provoquent pas de maladie virale chez l’homme et ne déclenchent généralement pas de réponse immunitaire, ce qui dégraderait rapidement leur impact thérapeutique.
Les AAV et les transgènes thérapeutiques qu’ils peuvent transporter existent normalement de manière « épisomique » : flottant librement dans le noyau cellulaire et non intégrés dans l’ADN chromosomique. Cependant, les scientifiques reconnaissent désormais que les AAV modifiés utilisés pour les thérapies géniques finissent parfois dans l’ADN chromosomique, peut-être principalement en raison de processus de réparation de l’ADN qui les assemblent par inadvertance dans le génome.
Certaines études sur les thérapies géniques AAV dirigées vers le foie chez la souris, en particulier chez la souris nouveau-née, ont montré que ces insertions peuvent déclencher un cancer du foie en perturbant les éléments régulateurs bloquant le cancer dans le génome. On ne sait pas exactement si cela est susceptible de se produire chez les humains et d’autres primates.
Dans le Thérapie génique humaine Dans cette étude, les chercheurs de Penn ont examiné des échantillons de tissus, principalement des échantillons de foie, provenant de 86 singes macaques qui avaient été traités avec des thérapies géniques à base d’AAV lors de tests précliniques, et de 253 macaques et humains qui n’avaient jamais été exposés à des AAV modifiés.
Ils ont constaté que les AAV modifiés chez les bénéficiaires de thérapie génique et les AAV endémiques naturels (« de type sauvage ») dans l’autre groupe, étaient insérés à de faibles taux dans des distributions principalement aléatoires à travers le génome avec un faible risque d’expansion, même dans un singe 15 ans après le traitement.
Dans le Biotechnologie naturelle Dans cette étude, l’équipe de Wilson a suivi 12 macaques pendant plus de 2 ans après qu’ils aient reçu des thérapies géniques basées sur l’AAV ciblant les cellules hépatiques.
Ils ont découvert la présence de structures complexes de génomes d’AAV existant en dehors du chromosome qui persistent mais semblent être rapidement inactivées peu après la délivrance du vecteur. Des formes intégrées d’ADN vectoriel sont apparues à des fréquences plus basses, ce qui correspond au nombre de cellules exprimant le transgène de manière stable, ce qui suggère que la durabilité de la thérapie génique AAV dans le foie des primates pourrait être due aux formes intégrées du vecteur.
Une fois de plus, ils ont découvert une faible fréquence de séquences de vecteurs AAV intégrées dans l’ADN chromosomique, à différents sites du génome. Aucun de ces sites n’était proche de gènes dont la perturbation a été liée au cancer du foie, et il n’y avait aucune preuve d’expansion clonale marquée au cours des années de suivi.
“Ces études éclairent de nouvelles approches pour améliorer la thérapie génique hépatique qui se concentrent davantage sur l’expression plutôt que sur la délivrance”, a déclaré l’auteur principal de l’étude, James M. Wilson, MD, Ph.D., directeur du programme de thérapie génique, professeur Rose H. Weiss et Directeur de l’Orphan Disease Center et professeur aux départements de médecine et de pédiatrie de la Perelman School of Medicine de l’Université de Pennsylvanie.
“Nos données mettent également en évidence les avantages potentiels de l’édition du génome pour le foie dans laquelle les insertions sont dirigées vers des régions de refuge du chromosome au-dessus du fond d’intégrations plus largement distribuées qui se produisent avec le vecteur seul.”
Plus d’information:
Greig, JA et al, Les génomes de vecteurs intégrés peuvent contribuer à l’expression à long terme dans le foie des primates après l’administration d’AAV, Biotechnologie naturelle (2023). DOI : 10.1038/s41587-023-01974-7 www.nature.com/articles/s41587-023-01974-7
Thérapie génique humaine(2023). DOI : 10.1089/hum.2023.134
Fourni par la Perelman School of Medicine de l’Université de Pennsylvanie
Citation: Les thérapies géniques basées sur l’AAV chez les primates non humains suggèrent que l’intégration dans l’ADN humain est peu susceptible de conduire à des mutations cancéreuses (6 novembre 2023) récupéré le 6 novembre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.