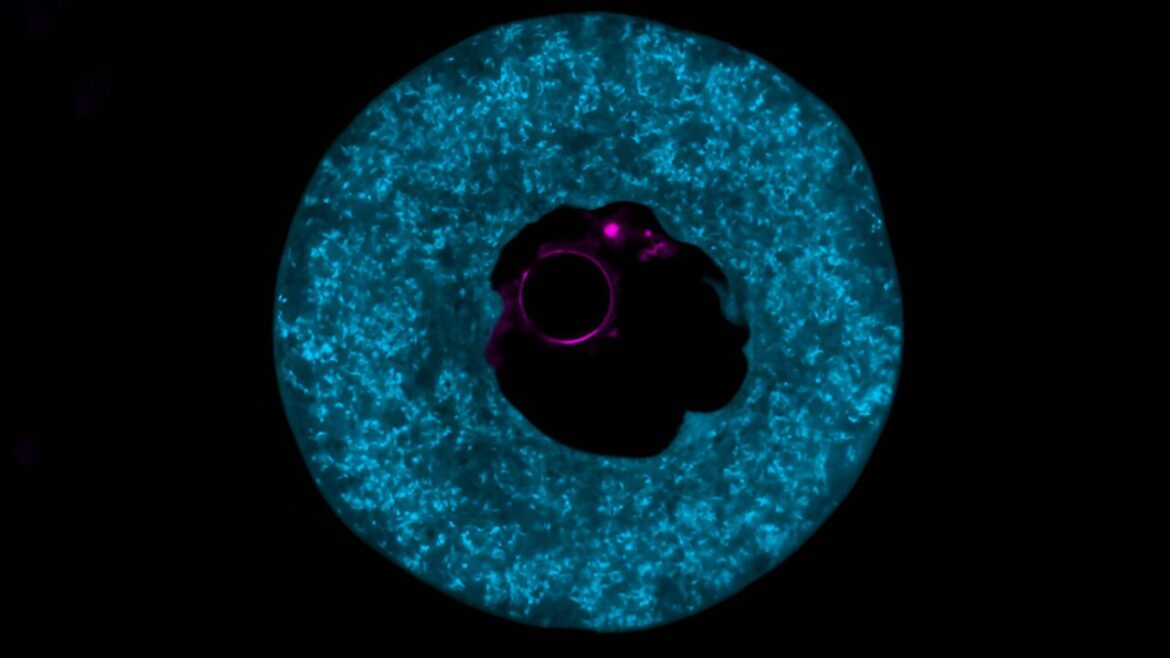
Un ovule de souris, naturellement rempli de la protéine PADI6 (bleue), marqueur et composant principal du réseau cytoplasmique. L’ADN du noyau cellulaire est représenté en magenta. Crédit : MPI f. Sciences multidisciplinaires/ Ida Marie Astad Jentoft
Lorsque les mammifères ont une progéniture, ils investissent beaucoup. Contrairement aux poissons ou aux grenouilles, l’embryon ne peut pas se développer tout seul. Il doit s’implanter dans l’utérus, où il reçoit tout ce dont il a besoin pour survivre. En attendant, l’ovule nourrit le premier embryon. Il apporte entre autres des protéines essentielles.
Les chercheurs dirigés par Melina Schuh de l’Institut Max Planck pour les sciences multidisciplinaires, en collaboration avec des collègues de Göttingen, ont maintenant élucidé comment les ovules stockent les protéines. Leurs expériences fournissent également des informations importantes sur la manière dont les erreurs de stockage des protéines peuvent conduire à l’infertilité. Les structures de l’ovule, qui intriguent les scientifiques depuis plus de 60 ans, jouent un rôle crucial à cet égard. L’ouvrage est publié dans la revue Cellule.
Pour de nombreux couples, la parentalité tarde à venir. Pour certains, le désir d’avoir des enfants reste même inassouvi. Les causes sont variées et peuvent se retrouver aussi bien chez les hommes que chez les femmes. Chez les femmes, la fertilité diminue avec l’âge et l’infertilité devient plus probable. Cependant, des mutations génétiques peuvent également y contribuer.
Les analyses du matériel génétique des femmes infertiles dans le monde entier ont montré que l’une des causes génétiques les plus courantes de l’infertilité féminine est la mutation de certains gènes. Ceux-ci contiennent les plans de la protéine PADI6 et du complexe protéique Subcortial Maternal Complex, ou SCMC en abrégé. Cependant, on ne savait pas encore clairement quel rôle ces protéines jouent en particulier dans l’infertilité.

Ida Jentoft (à droite) et Melina Schuh travaillant sur un microscope optique. Crédit : MPI f. Sciences multidisciplinaires/ Swen Pförtner
Site de stockage de protéines pour le jeune embryon
Les scientifiques dirigés par Melina Schuh ont maintenant utilisé des techniques d’imagerie pour visualiser que PADI6 et SCMC sont les principaux composants des structures qui remplissent l’intérieur de l’ovule. “Le monde de la recherche s’interroge depuis des décennies sur la fonction et la composition de cette structure, que nous appelons réseaux cytoplasmiques”, explique Schuh, directeur de Max Planck.
Lorsque les scientifiques ont retiré les protéines PADI6 et SCMC des ovules de souris, le réseau cytoplasmique a été perdu, avec des conséquences fatales. “Les ovules de souris dépourvus de réseaux cytoplasmiques manquaient également des protéines nécessaires au jeune embryon. Le développement de l’embryon s’est arrêté peu de temps après la fécondation”, explique le biologiste cellulaire. “Nous soupçonnions donc que les réseaux cytoplasmiques pourraient servir de sites de stockage de protéines.”
Le stockage des protéines dans l’ovule n’est en aucun cas anodin. En effet, les ovules sont créés dans les ovaires d’une femelle mammifère dès la naissance et y restent fonctionnels pendant des mois, voire des années. Les ovules doivent conserver leurs protéines en stock pendant une période de temps correspondante sans se dégrader ni devenir actives au mauvais moment.
Dans l’étape suivante, les chercheurs ont étudié quelles protéines sont contenues dans les réseaux cytoplasmiques. En coopération avec des groupes dirigés par Henning Urlaub et Juliane Liepe de l’Institut Max Planck, ils ont utilisé la spectrométrie de masse et la bioinformatique pour déterminer l’inventaire exact des protéines des réseaux.
Comme les résultats l’ont montré, les réseaux cytoplasmiques se lient à de nombreuses protéines essentielles au développement embryonnaire. “Nos résultats indiquent clairement que notre hypothèse est correcte : les réseaux cytoplasmiques sont les sites de stockage des protéines de l’ovule et fournissent au jeune embryon des protéines vitales”, souligne Schuh.
Les protéines PADI6 et SCMC stockent les protéines
Comme ils l’ont découvert en outre, les protéines PADI6 et SCMC assument la tâche de collecter et de stocker les protéines nécessaires au développement précoce de l’embryon. “Cela explique pourquoi les embryons cessent de se développer peu de temps après la fécondation si ces protéines manquent ou ne peuvent pas remplir leur fonction”, explique Ida Jentoft, première auteure de l’étude. “Nous souhaitions ensuite savoir si un site de stockage de protéines défectueux pouvait être remplacé si, par exemple, PADI6 et SCMC manquaient en raison de mutations génétiques.”
Lors d’expériences, l’équipe a réussi à réintroduire artificiellement les protéines de réseau manquantes dans les ovules de souris en croissance. Avec cette approche, il pourrait également être possible de reconstruire le réseau cytoplasmique des ovules humains défectueux. Selon Jentoft, cela pourrait constituer une nouvelle approche prometteuse pour traiter l’infertilité causée par des mutations des gènes PADI6 et SCMC.
Des ovocytes congelés au microscope
Lorsqu’on leur demande pourquoi il a fallu tant de décennies pour déchiffrer la fonction des structures en treillis énigmatiques dans l’ovule, Schuh et Jentoft ont une réponse courte : la taille de l’ovule et le manque de méthodes. Les ovules sont les géants parmi les différents types de cellules chez les mammifères. Ce qui les prédestine au stockage des protéines rend difficile la recherche à l’intérieur.
« Le défi méthodologique majeur était de rendre les ovules accessibles aux méthodes d’imagerie que nous avons utilisées : microscopie optique haute résolution et cryo-tomographie électronique (cryo-ET). Cette dernière permet d’examiner les structures moléculaires de l’ovule en 3D. dans des conditions presque naturelles. Cela n’était pas possible jusqu’à présent”, explique le directeur de Max Planck. La percée de l’équipe dans cette procédure a été facilitée par une astuce éprouvée de la médecine reproductive.
Pour la cryo-ET, les cellules doivent d’abord être congelées par choc. Les chercheurs ont profité du fait que les cliniques congèlent régulièrement les ovules humains destinés à l’insémination artificielle pour les conserver. Pour protéger les ovules pendant la congélation, les cliniques utilisent des cryoprotecteurs. “Nous avons eu l’idée d’utiliser les mêmes cryoprotecteurs pour obtenir la congélation rapide requise des ovules”, rapporte Rubén Fernández-Busnadiego du centre médical universitaire de Göttingen.
“Grâce à cette technique, nous pouvons examiner les réseaux cytoplasmiques de l’ovule et commencer à déchiffrer leur structure en détail”, ajoute Schuh. Les scientifiques espèrent que les nouvelles techniques mèneront à des avancées importantes dans la recherche sur les ovocytes ainsi qu’à de nouvelles approches thérapeutiques à l’avenir.
Plus d’information:
Ida MA Jentoft et al, Les ovocytes de mammifères stockent des protéines pour l’embryon précoce sur des réseaux cytoplasmiques, Cellule (2023). DOI : 10.1016/j.cell.2023.10.003
Informations sur la revue :
Cellule
Fourni par la Société Max Planck
Citation: Comment les ovules stockent les protéines pour le début d’une nouvelle vie (6 novembre 2023) récupéré le 6 novembre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.