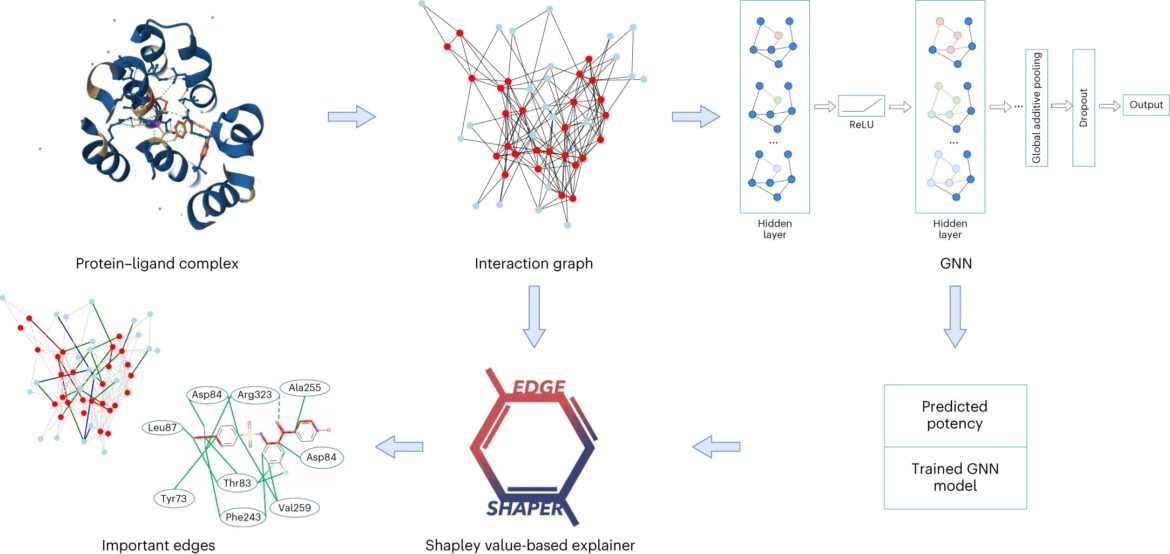
Rationalisation des prédictions d’affinité basées sur des graphiques d’interaction protéine-ligand. La représentation schématique résume les différentes étapes de l’analyse, y compris la génération de graphiques d’interaction à partir de structures à rayons X pour entraîner et tester un GNN afin de prédire les valeurs d’affinité numériques, suivie de la détermination de l’importance des bords pour les prédictions et de la délimitation des sous-graphiques déterminant les prédictions. Crédit: Intelligence des machines naturelles (2023). DOI:10.1038/s42256-023-00756-9
Quelle molécule médicamenteuse est la plus efficace ? Les chercheurs recherchent fébrilement des substances actives efficaces pour lutter contre les maladies. Ces composés s’ancrent souvent sur des protéines, qui sont généralement des enzymes ou des récepteurs qui déclenchent une chaîne spécifique d’actions physiologiques.
Dans certains cas, certaines molécules sont également destinées à bloquer des réactions indésirables dans l’organisme, comme une réponse inflammatoire excessive. Compte tenu de l’abondance des composés chimiques disponibles, cette recherche revient à première vue à chercher une aiguille dans une botte de foin. La découverte de médicaments tente donc d’utiliser des modèles scientifiques pour prédire quelles molécules s’arrimeront le mieux à la protéine cible respective et se lieront fortement. Ces candidats médicaments potentiels sont ensuite étudiés plus en détail dans le cadre d’études expérimentales.
Depuis les progrès de l’IA, la recherche sur la découverte de médicaments utilise également de plus en plus d’applications d’apprentissage automatique. Les « réseaux de neurones graphiques » (GNN) offrent l’une des nombreuses opportunités pour de telles applications. Ils sont adaptés pour prédire, par exemple, la force avec laquelle une certaine molécule se lie à une protéine cible.
À cette fin, les modèles GNN sont entraînés avec des graphiques représentant des complexes formés entre des protéines et des composés chimiques (ligands). Les graphiques sont généralement constitués de nœuds représentant des objets et d’arêtes représentant les relations entre les nœuds. Dans les représentations graphiques des complexes protéine-ligand, les arêtes connectent uniquement les nœuds protéine ou ligand, représentant respectivement leurs structures, ou les nœuds protéine et ligand, représentant des interactions protéine-ligand spécifiques.
“La façon dont les GNN parviennent à leurs prédictions est comme une boîte noire que nous ne pouvons pas entrevoir”, explique le professeur Jürgen Bajorath. Le chercheur en chimioinformatique de l’Institut LIMES de l’Université de Bonn, du Centre international des technologies de l’information de Bonn-Aix-la-Chapelle (B-IT) et de l’Institut Lamarr pour l’apprentissage automatique et l’intelligence artificielle de Bonn, en collaboration avec des collègues de l’Université Sapienza de Rome, a analysé en détail si les réseaux de neurones graphiques apprennent réellement les interactions protéine-ligand pour prédire la force avec laquelle une substance active se lie à une protéine cible.
La recherche est publiée dans Intelligence des machines naturelles.
Comment fonctionnent les applications d’IA ?
Les chercheurs ont analysé un total de six architectures GNN différentes à l’aide de leur méthode « EdgeSHAPer » spécialement développée et d’une méthodologie de comparaison conceptuellement différente. Ces programmes informatiques « examinent » si les GNN apprennent les interactions les plus importantes entre un composé et une protéine et prédisent ainsi la puissance du ligand, comme prévu et anticipé par les chercheurs, ou si l’IA parvient à ces prédictions par d’autres moyens.
“Les GNN dépendent beaucoup des données avec lesquelles ils sont formés”, explique le premier auteur de l’étude, Ph.D. le candidat Andrea Mastropietro de l’Université Sapienza de Rome, qui a mené une partie de ses recherches doctorales dans le groupe du professeur Bajorath à Bonn.
Les scientifiques ont formé les six GNN avec des graphiques extraits de structures de complexes protéine-ligand, pour lesquels le mode d’action et la force de liaison des composés à leurs protéines cibles étaient déjà connus grâce aux expériences. Les GNN formés ont ensuite été testés sur d’autres complexes. L’analyse EdgeSHAPer qui a suivi a ensuite permis de comprendre comment les GNN généraient des prédictions apparemment prometteuses.
“Si les GNN font ce qu’on attend d’eux, ils doivent apprendre les interactions entre le composé et la protéine cible et les prédictions doivent être déterminées en donnant la priorité aux interactions spécifiques”, explique le professeur Bajorath. Toutefois, selon les analyses de l’équipe de recherche, les six GNN n’y sont pour l’essentiel pas parvenus.
La plupart des GNN n’ont appris que quelques interactions protéine-médicament et se sont principalement concentrés sur les ligands. Bajorath explique : « Pour prédire la force de liaison d’une molécule à une protéine cible, les modèles se souvenaient principalement des molécules chimiquement similaires qu’ils avaient rencontrées au cours de l’entraînement et de leurs données de liaison, quelle que soit la protéine cible. Ces similitudes chimiques apprises déterminaient alors essentiellement la force de liaison d’une molécule à une protéine cible. prédictions.”
Selon les scientifiques, cela rappelle en grande partie « l’effet Clever Hans ». Cet effet fait référence à un cheval qui pourrait apparemment compter. La fréquence à laquelle Hans tapait du sabot était censée indiquer le résultat d’un calcul. Cependant, comme il s’est avéré plus tard, le cheval n’était pas du tout capable de calculer, mais il déduisait les résultats attendus des nuances des expressions faciales et des gestes de son compagnon.
Que signifient ces résultats pour la recherche sur la découverte de médicaments ? “Il n’est généralement pas tenable que les GNN apprennent les interactions chimiques entre les substances actives et les protéines”, explique le chimiste informatique.
Leurs prévisions sont largement surfaites car des prévisions de qualité équivalente peuvent être réalisées en utilisant des connaissances chimiques et des méthodes plus simples. Cependant, la recherche offre également des opportunités pour l’IA.
Deux des modèles examinés par GNN ont montré une nette tendance à apprendre davantage d’interactions lorsque la puissance des composés testés augmentait. “Cela vaut la peine d’y regarder de plus près”, déclare Bajorath. Peut-être que ces GNN pourraient être encore améliorés dans la direction souhaitée grâce à des représentations modifiées et à des techniques de formation.
Cependant, l’hypothèse selon laquelle les grandeurs physiques peuvent être apprises sur la base de graphiques moléculaires doit généralement être traitée avec prudence. “L’IA n’est pas de la magie noire”, déclare Bajorath.
En fait, il considère la précédente publication en libre accès d’EdgeSHAPer et d’autres outils d’analyse spécialement développés comme des approches prometteuses pour faire la lumière sur la boîte noire des modèles d’IA. L’approche de son équipe se concentre actuellement sur les GNN et les nouveaux « modèles de langage chimique ».
“Le développement de méthodes permettant d’expliquer les prédictions de modèles complexes constitue un domaine important de la recherche en IA. Il existe également des approches pour d’autres architectures de réseau, telles que des modèles de langage, qui aident à mieux comprendre comment l’apprentissage automatique parvient à ses résultats”, explique Bajorath.
Il s’attend à ce que des choses passionnantes se produisent bientôt également dans le domaine de « l’IA explicable » à l’Institut Lamarr, où il est chercheur principal et titulaire de la chaire d’IA dans les sciences de la vie.
Plus d’information:
Mastropietro, A. et al, Caractéristiques d’apprentissage des réseaux de neurones graphiques prédisant les affinités protéine-ligand, Intelligence des machines naturelles (2023). DOI : 10.1038/s42256-023-00756-9. www.nature.com/articles/s42256-023-00756-9
Fourni par la Rheinische Friedrich-Wilhelms-Universität Bonn
Citation: L’intelligence artificielle pour la découverte de médicaments offre des résultats inattendus (13 novembre 2023) récupéré le 13 novembre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.