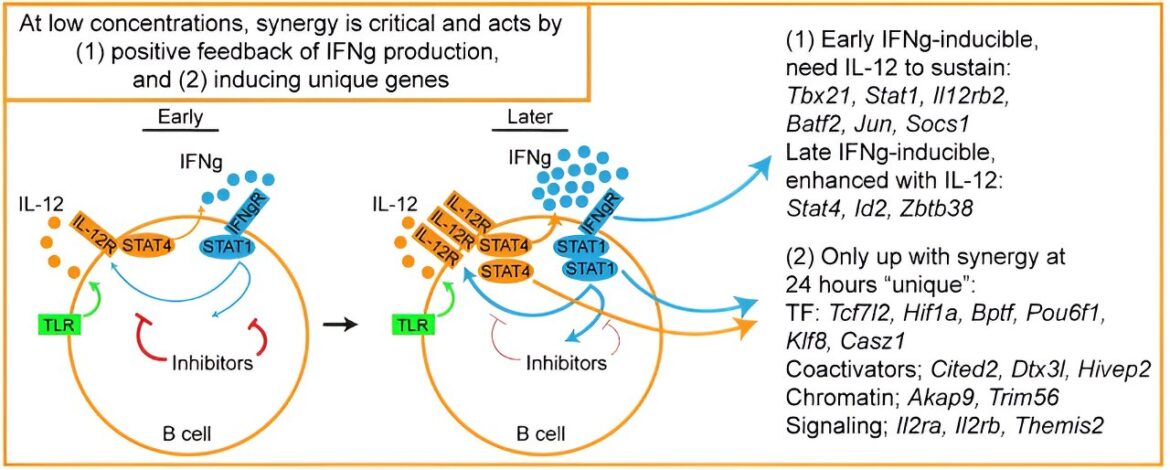
Représentation visuelle du modèle proposé. Au début (4 heures), l’IL-12 initie la production d’IFNγ et les signaux autocrines d’IFNγ induisent l’expression de gènes qui établissent à la fois une rétroaction négative de la signalisation IFNγ et une boucle de rétroaction positive se chevauchant entre la signalisation IL-12 et IFNγ. L’IFNγ favorise la signalisation de l’IL-12 en régulant positivement les composants de signalisation de l’IL-12 (IL-12R et STAT4) et STAT1 par lesquels l’IFNγ transmet le signal. Au bout de 24 heures, si l’IL-12 et l’IFNγ sont présents, une rétroaction positive surmonte la régulation négative pour maintenir la signalisation de l’IFNγ. De plus, l’IL-12 et l’IFNγ entrent en synergie pour induire des gènes qui ne sont exprimés dans aucune des deux conditions seules. Crédit: Immunologie naturelle (2024). DOI: 10.1038/s41590-024-01858-1
On sait que les lymphocytes B génèrent des anticorps via deux réponses différentes : une « réponse d’urgence » et une « tout va bien, préparons-nous à la réponse future », explique Mark Shlomchik, professeur à l’UPMC et professeur émérite d’immunologie à la faculté de médecine de l’Université de Pittsburgh. .
Cependant, les mécanismes biologiques qui coordonnent ces réponses sont restés un mystère pendant des décennies, jusqu’à aujourd’hui. Dans une étude publiée le 11 juin dans Immunologie naturelleShlomchik et Rebecca Elsner, premier auteur et professeur adjoint de recherche dans le laboratoire de Shlomchik, partagent leur découverte selon laquelle une cytokine appelée interleukine-12 (IL-12) agit comme un commutateur pour diriger la réponse en anticorps que les cellules B généreront.
Les deux réponses des lymphocytes B sont biologiquement importantes car chacune a un objectif différent. La « réponse d’urgence » (réponse extrafolliculaire) est la réaction immédiate du corps à une infection, dans laquelle les cellules B génèrent une abondance d’anticorps pour tenter de contrôler l’infection.
En revanche, la réponse « tout va bien » (centre germinal) est la reconnaissance par le corps d’une infection sous contrôle où il crée une mémoire de l’agent pathogène incriminé par le biais de cellules B mémoire et d’anticorps spécifiques de l’agent pathogène. Cette mémoire protégera le corps de toute infection ultérieure.
Comprendre ce qui active chaque réponse permettrait aux chercheurs de concevoir des vaccins capables de provoquer la réaction immunitaire souhaitée. Par exemple, dans le cas d’une infection grave, fournir un vaccin qui active la réponse extrafolliculaire pourrait aider un patient à survivre. Si une mémoire pathogène à long terme est nécessaire, le vaccin serait conçu pour induire une réponse du centre germinal. Cependant, ce contrôle nécessite de connaître ce qui fait que ces processus se produisent au niveau biologique.
“Vous ne pouvez pas conduire une voiture sans connaître les commandes et leur fonctionnement”, explique Shlomchik.
Après avoir découvert que l’IL-12 jouait un rôle dans l’inhibition de la réponse du centre germinal via les cellules T, leur récente découverte montre que l’IL-12 agit également pour pousser les cellules B vers une réponse extrafolliculaire. Dirigés par des niveaux élevés d’IL-12, les lymphocytes B produisent de l’interféron gamma et davantage d’IL-12 pour créer une boucle de rétroaction positive autocrine qui verrouille la décision de réponse extrafolliculaire.
“Ce commutateur d’IL-12 nous permet de comprendre comment contrôler ces deux types de réponses immunitaires à notre avantage”, explique Elsner.
En plus du contrôle du type de réponse, ce commutateur d’IL-12 peut également aider les enquêteurs à comprendre quand et pourquoi les réponses immunitaires tournent mal. En apprenant à contrôler ce changement, les chercheurs peuvent potentiellement affiner la réponse extrafolliculaire lorsque les vaccins ne fonctionnent pas comme prévu. De plus, la capacité de réduire la réponse extrafolliculaire en désactivant l’IL-12 pourrait constituer une nouvelle approche du traitement des maladies auto-immunes.
Plus d’information:
Rebecca A. Elsner et al, IL-12 induit une boucle de rétroaction IL-12/IFNγ intrinsèque aux cellules B favorisant les réponses extrafolliculaires des cellules B, Immunologie naturelle (2024). DOI : 10.1038/s41590-024-01858-1
Fourni par l’Université de Pittsburgh
Citation: Décisions de changement : l’interleukine-12 influence la réponse immunitaire des cellules B (27 juin 2024) récupéré le 27 juin 2024 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.