Crédit: Rapports cellulaires Médecine (2024). DOI : 10.1016/j.xcrm.2024.101606
La maladie leptoméningée est une complication rare mais mortelle rencontrée par les patients atteints d'un mélanome à un stade avancé. Cela se produit lorsque les cellules cancéreuses se propagent aux membranes recouvrant le cerveau et la moelle épinière, ou les leptoméninges. Cette pathologie, qui touche 5 à 8 % des patients atteints de mélanome, entraîne souvent une détérioration rapide et est notoirement résistante aux thérapies. Cependant, une nouvelle étude du Moffitt Cancer Center, publiée dans Rapports cellulaires Médecinedécouvre les mécanismes à l'origine de cette résistance aux médicaments, offrant ainsi de nouvelles pistes de traitements potentiels.
Les chercheurs de Moffitt ont analysé des échantillons de tissus provenant de patients atteints d'une maladie leptoméningée et les ont comparés à des métastases provenant d'autres parties du corps chez les mêmes individus. Ils ont découvert que les cellules de mélanome des leptoméninges interagissent de manière significative avec les cellules stromales. Dans des conditions saines, les cellules stromales jouent un rôle crucial dans le maintien de la santé et du fonctionnement de divers tissus et organes du corps. Dans les métastases leptoméningées du mélanome, les interactions entre ces cellules stromales et la tumeur activent des signaux favorisant la tumeur.
« Comprendre l'environnement unique des métastases leptoméningées dans le mélanome a été un défi majeur. Nos résultats démontrent que les cellules stromales « normales » dans les leptoméninges jouent un rôle crucial dans le soutien de la croissance tumorale et de la résistance aux inhibiteurs de MAPK, un traitement courant du mélanome », a déclaré Inna Smalley, Ph.D., auteure principale, membre adjointe du Département de métabolisme et de physiologie et membre du Centre d'excellence Donald A. Adam sur le mélanome et le cancer de la peau.
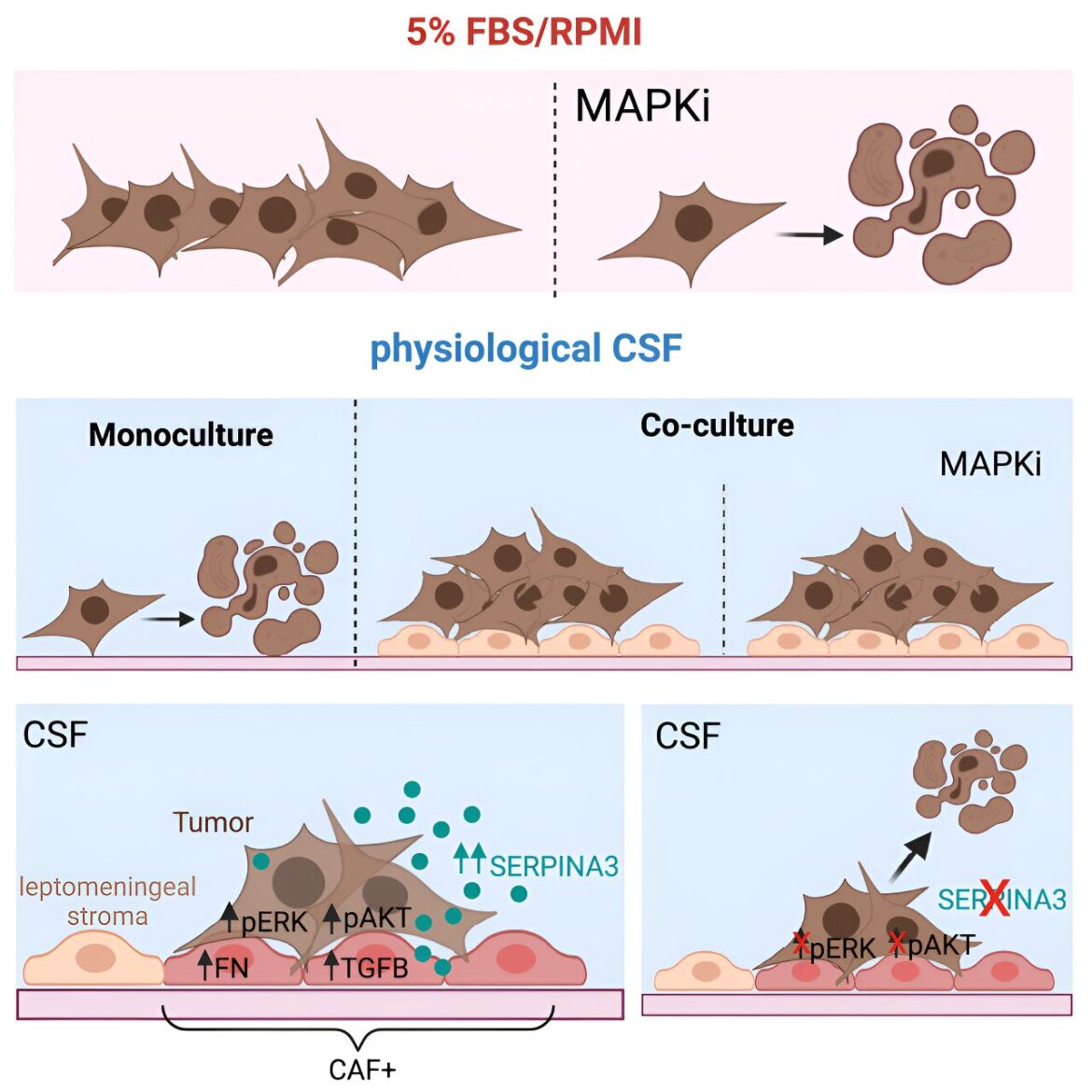
L'analyse transcriptomique spatiale de pointe des chercheurs a révélé des voies de signalisation spatiales associées à la croissance du mélanome et à la résistance aux médicaments, en particulier dans les régions où les cellules tumorales et stromales interagissent. Ils ont identifié la protéine SERPINA3 comme régulateur des interactions tumeur-stroma, suggérant une cible potentielle pour une intervention thérapeutique.
“Nos données suggèrent que cibler l'interaction tumeur-stroma, en particulier par l'inhibition de la signalisation médiée par SERPINA3, pourrait représenter une nouvelle stratégie pour vaincre la résistance aux médicaments dans le mélanome leptoméningé”, a déclaré Smalley. “En perturbant cette interaction critique, nous pourrons peut-être améliorer l'efficacité des thérapies existantes et améliorer les résultats pour les patients.”
L'étude a également mis en évidence les défis métaboliques uniques des cellules de mélanome dans le liquide céphalo-rachidien. L’équipe a démontré que le stroma méningé est essentiel à la survie des cellules de mélanome dans cet environnement hostile, soulignant ainsi l’importance de l’interaction tumeur-stroma.
Plus d'information:
Hasan Alhaddad et al, L'analyse transcriptomique spatiale identifie une fonction favorisant la tumeur du stroma méningé dans la maladie leptoméningée du mélanome, Rapports cellulaires Médecine (2024). DOI : 10.1016/j.xcrm.2024.101606
Fourni par le Centre de cancérologie et institut de recherche H. Lee Moffitt
Citation: Une étude révèle un nouveau mécanisme de résistance aux médicaments dans le mélanome leptoméningé (11 juin 2024) récupéré le 11 juin 2024 sur
Ce document est soumis au droit d'auteur. En dehors de toute utilisation équitable à des fins d'étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.