Crédit: Biologie chimique cellulaire (2023). DOI : 10.1016/j.chambiol.2023.11.008
Une équipe du Children's Medical Research Institute a découvert une nouvelle façon d'altérer la croissance des cellules cancéreuses, ce qui pourrait conduire au développement d'une nouvelle classe de traitements contre le cancer avec des effets secondaires minimes sur les cellules normales.
Le professeur Hilda Pickett, qui dirige l'unité de régulation de la longueur des télomères du CMRI, a déclaré qu'il s'agissait d'un développement passionnant pour leur équipe.
“Ce projet s'appuie sur plus d'une décennie de travail de mon équipe et de nos collaborateurs pour développer des agents antiprolifératifs ciblant les télomères. Les résultats sont prometteurs et pourraient potentiellement améliorer les résultats de santé à long terme pour tous les types de cancer”, déclare Pickett.
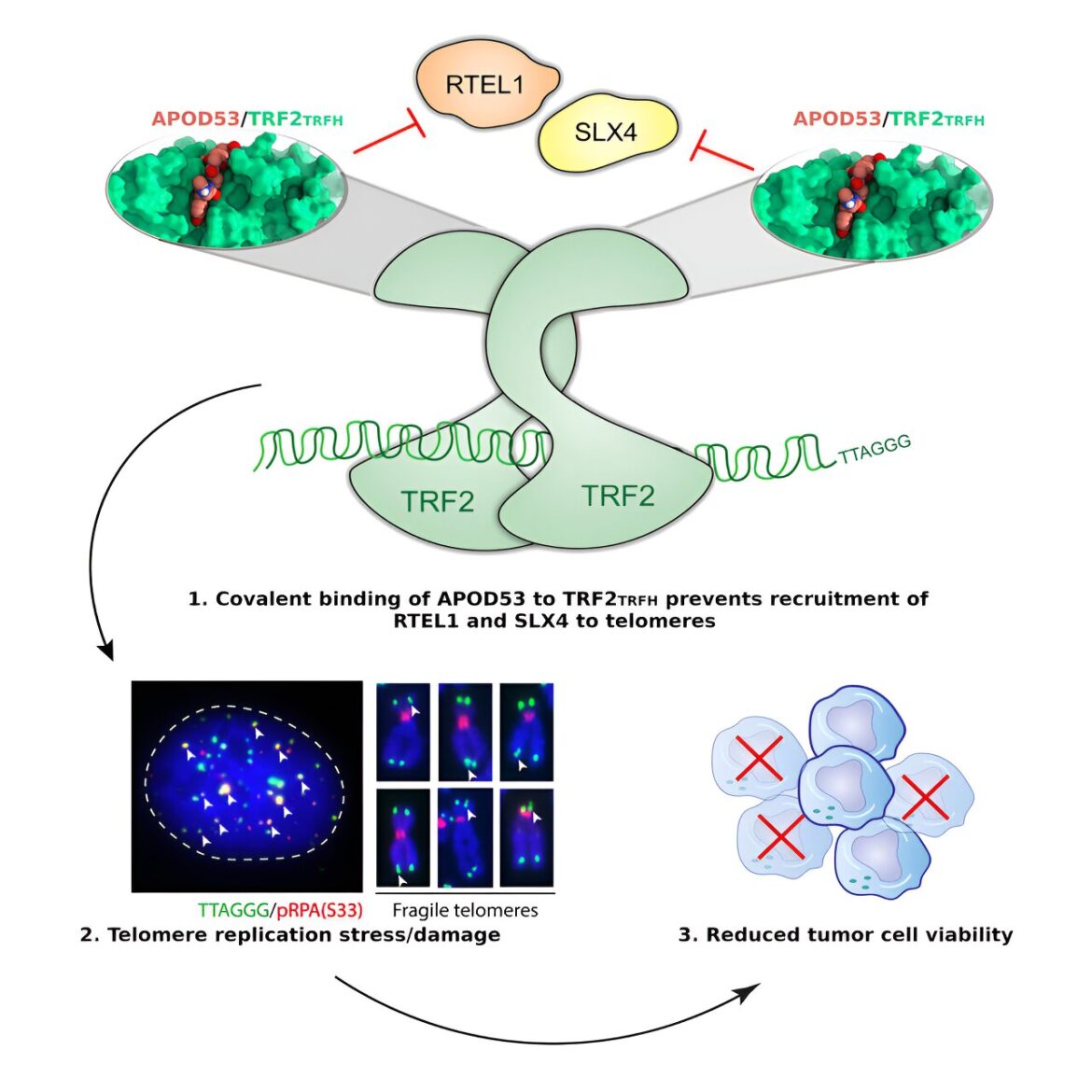
Notre ADN est protégé par des télomères, situés aux extrémités de nos chromosomes, qui forment une structure en boucle gardée par un ensemble de protéines, l'une des plus cruciales étant TRF2. Lorsque cette structure protectrice des télomères est perturbée, des effets catastrophiques se produisent sur les cellules, entraînant leur mort.
Les cellules cancéreuses existent au bord de la catastrophe. La capacité de prolifération illimitée des cellules cancéreuses dépend entièrement du maintien des télomères, ce qui fait des facteurs qui contrôlent les télomères des cibles chimiothérapeutiques attrayantes. Tout ce qui les fait basculer peut tuer sélectivement les cellules cancéreuses sans nuire aux cellules normales de notre corps. Contrairement à la radiothérapie et à la plupart des chimiothérapies, les effets secondaires des médicaments anticancéreux axés sur les télomères devraient être beaucoup plus faibles, améliorant ainsi la survie des patients et les résultats à long terme.
Le Dr Alex Sobinoff du CMRI, membre de l'équipe du professeur Pickett, est l'auteur principal d'un article publié dans Biologie chimique cellulaire, qui décrit le premier composé à se lier fortement à une région clé de TRF2. Ce composé, appelé APOD53, altère la croissance cellulaire des cellules cancéreuses (en utilisant les deux mécanismes connus de maintenance des télomères : ALT et télomérase), tout en épargnant les cellules non cancéreuses.
“Ces composés représentent de nouveaux outils fantastiques pour la recherche fondamentale et prouvent que nous pouvons développer des traitements anticancéreux ciblant spécifiquement TRF2”, déclare Sobinoff.
Ils ont également montré que l'efficacité de leur nouveau composé peut être augmentée en combinaison avec d'autres produits chimiques affectant d'autres parties de la structure protectrice des télomères. De plus, leur composé, un peptide, est perméable, ce qui signifie qu'il peut facilement pénétrer dans les cellules et constitue donc un bon candidat pour le développement futur de médicaments anticancéreux.
“Le succès de ces composés à un stade précoce peut être attribué à l'approche de conception intelligente de médicaments que nous avons utilisée, combinée à notre compréhension approfondie de la biologie des télomères”, expliquent les chercheurs.
Plus d'information:
Alexander P. Sobinoff et al, L'inhibition irréversible des fonctions de recrutement de TRF2TRFH par un peptide cyclique covalent induit un stress de réplication télomérique dans les cellules cancéreuses, Biologie chimique cellulaire (2023). DOI : 10.1016/j.chambiol.2023.11.008
Fourni par l'Institut de recherche médicale pour enfants (CMRI)
Citation: Un nouveau composé pourrait conduire à des traitements qui tuent sélectivement les cellules cancéreuses (8 décembre 2023) récupéré le 8 décembre 2023 sur
Ce document est soumis au droit d'auteur. En dehors de toute utilisation équitable à des fins d'étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.