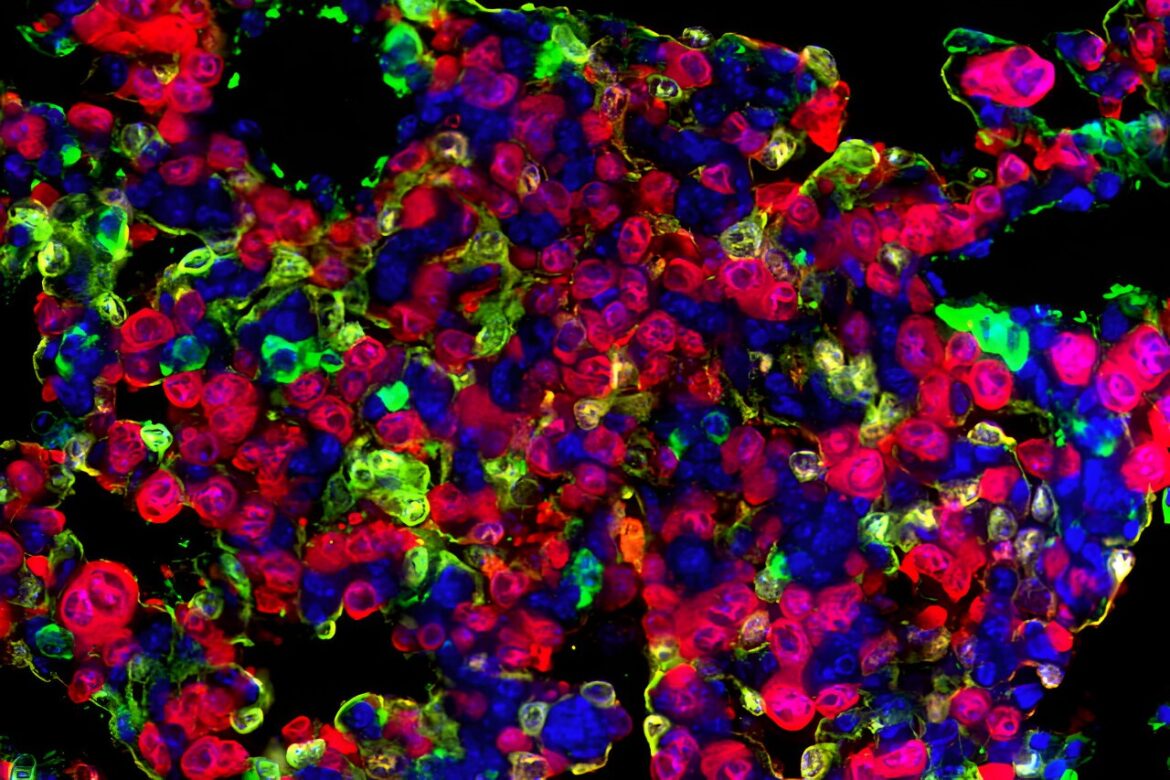
Les cellules cancéreuses du poumon (rouge) dans le poumon de la souris s’adaptent à l’inhibition de KRAS (vert). Cette adaptation permet aux cellules de résister au traitement par un inhibiteur de KRAS et peut entraîner une résurgence ultérieure du cancer du poumon. Crédit : Tammela Lab, Memorial Sloan Kettering Cancer Center
Une nouvelle compréhension des « mémoires » des cellules cancéreuses du poumon suggère une nouvelle stratégie pour améliorer le traitement, ont découvert les chercheurs du Memorial Sloan Kettering Cancer Center (MSK).
Recherche du laboratoire du biologiste du cancer Tuomas Tammela, MD, Ph.D. montre que certaines cellules cancéreuses du poumon conservent une « mémoire » de la cellule saine d’où elles proviennent – une mémoire qui pourrait être exploitée pour rendre plus efficace un type émergent de traitement du cancer du poumon appelé inhibition de KRAS.
L’étude a porté spécifiquement sur l’adénocarcinome du poumon, un type de cancer du poumon non à petites cellules qui est le type de cancer du poumon le plus courant aux États-Unis et responsable de 7 % de tous les décès par cancer. Ce cancer est souvent dû à des mutations du gène KRAS.
“Pendant longtemps, les protéines KRAS responsables du cancer ont été considérées comme ‘non médicamentables'”, explique Zhuxuan “Zoe” Li, co-premier auteur de l’étude, doctorant au laboratoire Tammela de l’institut Sloan Kettering de MSK. “Au cours des dernières années, cependant, la Food and Drug Administration des États-Unis a approuvé les premiers inhibiteurs de KRAS, et un certain nombre d’autres ont fait l’objet d’essais cliniques. Mais ils ne fonctionnent pas pour tout le monde et le cancer de la plupart des patients finit par acquérir une résistance aux médicaments. et reviens.”
Les découvertes de l’équipe, codirigées par le chercheur postdoctoral Xueqian Zhuang, Ph.D., jettent un éclairage important sur les cellules cancéreuses du poumon qui persistent après un traitement avec un inhibiteur de KRAS. Surtout, ils suggèrent que cibler séparément ces cellules parallèlement à un traitement avec un inhibiteur de KRAS pourrait aider à prévenir la récidive. L’étude a été récemment publiée dans Découverte du cancerune revue leader sur les connaissances biologiques ayant des implications importantes pour les soins cliniques.
Cellules souches avec un travail quotidien
Pour comprendre la découverte MSK et ses implications, il est utile de connaître un peu la biologie pulmonaire.
Dans les poumons, l’oxygène est absorbé et le dioxyde de carbone est libéré via des sacs aériens appelés alvéoles. La muqueuse des alvéoles est constituée de deux types distincts de cellules : le type alvéolaire 1 (AT1) et le type alvéolaire 2 (AT2).
Et même si elles portent le même nom, ces deux cellules ne pourraient pas être plus différentes.
Les cellules AT1 sont longues et fines, avec une grande surface pour faciliter les échanges gazeux entre les poumons et la circulation sanguine.
Les cellules AT2, quant à elles, jouent un rôle de gardien, en sécrétant des composés importants pour la santé et le fonctionnement des poumons, et en aidant à entretenir et à réparer les poumons en se divisant pour créer des cellules AT1 de remplacement.
“Vous pouvez les considérer comme des cellules souches avec un travail quotidien”, explique le Dr Tammela.
Le gros problème survient lorsque les cellules cancéreuses du poumon – qui se développent généralement à partir des cellules AT2 – acquièrent certaines propriétés « mémorisées » des cellules AT1 en lesquelles les cellules AT2 se différencient lorsqu’elles jouent leur rôle de cellule souche. Les scientifiques appellent ces cellules cancéreuses des cellules « de type AT1 ».
L’élimination des cellules de type AT1 améliore la réponse à l’inhibition de KRAS
Dans les cellules saines, KRAS joue un rôle clé dans la régulation de la croissance et de la division cellulaire. Mais lorsque le gène mute, cela peut entraîner une prolifération cellulaire incontrôlée.
Les inhibiteurs de KRAS peuvent arrêter cette croissance explosive, réduisant ainsi considérablement les tumeurs, mais ils laissent quand même des poches de cellules cancéreuses qui ne sont pas sensibles au médicament, ce qui donne également au cancer une chance de développer de nouvelles mutations pour résister aux effets des médicaments.
L’équipe de recherche a minutieusement étudié ces cellules cancéreuses résiduelles pour découvrir les mécanismes de cette résistance à l’aide de modèles de souris génétiquement modifiés, de souris implantées avec des tumeurs dérivées de patients et d’échantillons de tumeurs de patients.
Ils ont découvert que les cellules cancéreuses qui restaient après le traitement étaient des cellules de type AT1. Ils ont également découvert que ces cellules ont la capacité de relancer la croissance incontrôlée du cancer.
“Il est important de noter que nous avons constaté que si l’on se débarrasse de ces cellules de type AT1, la réponse au traitement aux inhibiteurs de KRAS s’améliore considérablement”, explique le Dr Tammela.
L’élimination de ces cellules dans des modèles expérimentaux est relativement facile, mais cela nécessitera des recherches plus approfondies.
“Nous vivons en fait à une époque très excitante avec une pharmacologie fantastique”, déclare le Dr Tammela. “Nous pouvons concevoir des molécules pour qu’elles se lient à un certain type de cellule et les tuent. C’est ainsi que fonctionnent la thérapie cellulaire CAR T et les conjugués anticorps-médicament.
“Maintenant que nous avons réalisé ces expériences de validation de principe, la prochaine étape consisterait à trouver des protéines de surface uniques à ces cellules de type AT1, puis à développer un médicament capable de s’y lier et de les tuer”, ajoute-t-il. .
Seulement dans un endroit comme MSK
Les collaborations avec d’autres laboratoires ont été essentielles à la recherche, explique le Dr Tammela.
“C’est le type de recherche qui ne peut réellement avoir lieu que dans un endroit comme MSK”, dit-il. “Nous avons eu des collaborations très importantes avec d’autres laboratoires de MSK qui partageaient des modèles animaux et des échantillons de patients qui faisaient partie intégrante de l’étude, et nous avons travaillé en étroite collaboration avec plusieurs des principales installations de MSK : le noyau d’évaluation antitumorale, l’opération de génomique intégrée, le noyau de cytométrie en flux et Noyau de cytologie moléculaire.”
Chercheurs MSK Scott Lowe, Ph.D. et Charles Rudin, MD, Ph.D. ont été des contributeurs clés, note le Dr Tammela.
“Et l’étude n’aurait pas été possible sans le dévouement de Zoé, sans les systèmes modèles et les premières connaissances développées par le Dr Zhuang”, ajoute-t-il.
Les autres auteurs incluent Chun-Hao Pan, Yan Yan, Rohit Thummalapalli, Stefan Torborg, Anupriya Singhal, Jason Chang et Rona Yaeger de MSK ; Simon Joost, anciennement de MSK et maintenant chez GC Therapeutics ; Eusebio Manchado, anciennement de MSK, aujourd’hui à l’Institut Novartis de recherche biomédicale ; Jill Hallin et James Christensen de Mirati Theraputics ; et Lukas Dow de Weill Cornell Medicine.
Plus d’information:
Zhuxuan Li et al, La différenciation alvéolaire entraîne la résistance à l’inhibition de KRAS dans l’adénocarcinome du poumon, Découverte du cancer (2023). DOI : 10.1158/2159-8290.CD-23-0289
Fourni par le Memorial Sloan Kettering Cancer Center
Citation: Les « souvenirs » des cellules cancéreuses du poumon suggèrent une nouvelle stratégie pour améliorer le traitement (18 novembre 2023) récupéré le 18 novembre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.