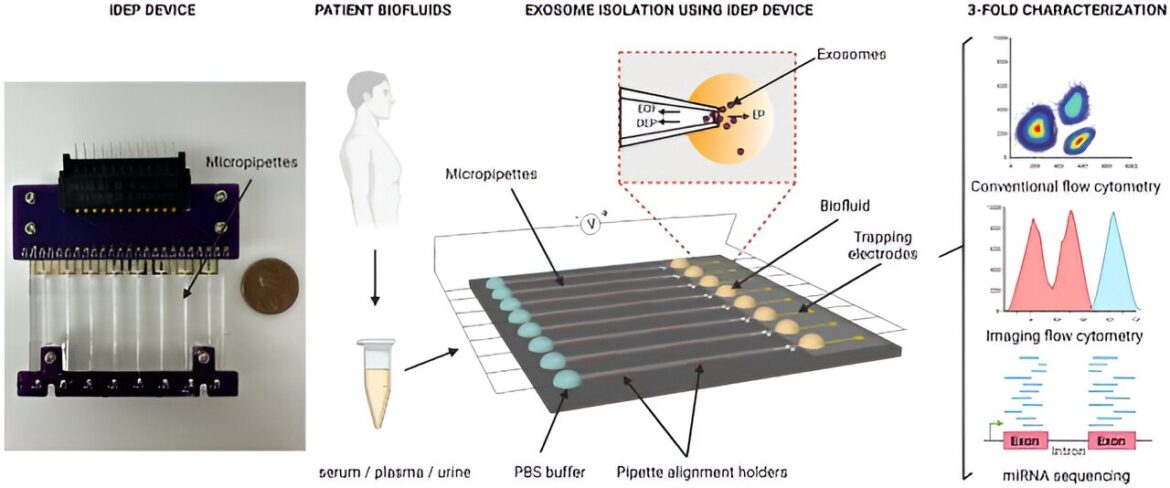
Disposition de l’appareil et aperçu graphique du flux expérimental. De petites vésicules extracellulaires (sEV) ont été extraites simultanément de biofluides humains à l’aide du dispositif diélectrophorétique à base d’isolant (iDEP), dans lequel une zone de piégeage a été créée au niveau de la pointe des micropipettes en équilibrant la force diélectrophorétique (DEP) avec deux forces électrocinétiques, y compris l’électroosmose. (EOF) et électrophorèse (EP). Les isolats de sEV ont été caractérisés de manière exhaustive à l’aide de la cytométrie en flux, d’ImageStreamx et du séquençage de microARN (miARN). Crédit: Rapports scientifiquesest ce que je: 10.1038/s41598-023-45409-4
Toutes les cellules sécrètent naturellement des vésicules extracellulaires à l’échelle nanométrique sous forme de particules délimitées par des bicouches lipidiques. Ce sont donc des biomarqueurs valables pour identifier diverses maladies.
Il est important d’isoler efficacement les petites vésicules extracellulaires tout en maintenant le rendement et la pureté pour explorer leur potentiel dans les applications diagnostiques, pronostiques et thérapeutiques.
Les méthodes conventionnelles d’isolement présentent des inconvénients, notamment une pureté et un rendement faibles, des procédures d’extraction longues, des équipements spécialisés et des coûts élevés.
Dans une étude publiée dans Rapports scientifiquesManju Sharma et une équipe de scientifiques en génie biomédical de l’Université de Cincinnati Ohio, États-Unis, ont développé un nouveau dispositif diélectrophorétique à base d’isolant pour isoler rapidement les petites vésicules extracellulaires des biofluides et des milieux de culture cellulaire, en fonction de leurs propriétés diélectriques.
Les scientifiques ont caractérisé les petites vésicules extracellulaires isolées des biofluides de patients atteints de cancer à l’aide de l’instrument et ont mené une triple caractérisation avec la cytométrie en flux conventionnelle, la cytométrie en flux par imagerie avancée et le séquençage de microARN pour obtenir un rendement élevé de vésicules extracellulaires pures. La plateforme est efficace pour isoler rapidement les biomarqueurs et maintenir l’intégrité biomoléculaire des vésicules.
Récipients biologiques encapsulés dans une membrane
Biologiquement, les petites vésicules extracellulaires sont des vaisseaux biologiques encapsulés dans une membrane que l’on trouve dans les biofluides tels que le sang, l’urine, la salive, le sperme, le lait maternel et le liquide céphalo-rachidien ; libéré par les cellules dans l’espace extracellulaire.
De telles vésicules à l’échelle nanométrique peuvent transférer horizontalement leur cargaison biomoléculaire pour fonctionner comme vecteurs de signalisation intercellulaire. De telles vésicules extracellulaires offrent un degré élevé de sensibilité et de spécificité en raison de leur excellente stabilité. Leur détection précoce dans les biopsies liquides peut améliorer la détection des cancers, des infections et des maladies neurodégénératives et métaboliques.
L’isolement des vésicules est cependant difficile en raison de leur taille nanométrique et de leurs propriétés physicochimiques. Les méthodes d’isolement dépendent généralement des propriétés des vésicules extracellulaires et, bien que ces dispositifs présentent des attributs prometteurs, leur coût de fabrication, la dilution des échantillons et leur sensibilité au colmatage constituent des défis inhérents.
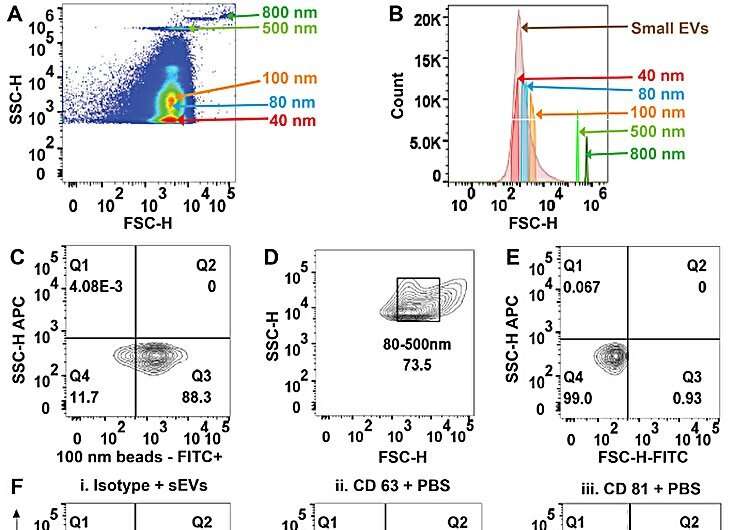
(A) FSC-H versus SSC-H de l’analyse des billes PS-COOH sur cytométrie en flux haute résolution représente la résolution de la taille des billes dans le mélange PS-COOH. (B) Histogramme illustrant différentes tailles de billes PS-COOH et de petites vésicules extracellulaires (sEV) dérivées du sérum. (C) Parcelles représentatives de billes PS-COOH-100 nm fluorescence-FITC. (D) Représentant FSC-H versus SSC-H des isolats de sEV du plasma humain. (E) Représentant FSC-H contre SSC-H de sEV non colorés démontrant le déclenchement. (F) Parcelles représentatives comme contrôles négatifs i. sEV colorés par isotype. ii. Anticorps CD63 dans du PBS et iii. Anticorps CD81 dans du PBS. (G) Parcelles de points représentatives de sEV colorées pour CD63 de i. sérum ii. plasma et iii. urine. (H) Parcelles représentatives de sEV colorées pour CD81 de i. sérum ii. plasma et iii. urine. Crédit: Rapports scientifiquesest ce que je: 10.1038/s41598-023-45409-4
En réponse, Sharma et ses collègues ont développé une nouvelle approche diélectrophorétique basée sur un isolant avec des micropiliers dans des canaux microfluidiques pour engloutir rapidement les nanoparticules en fonction de leur taille et de leurs propriétés diélectriques uniques.
Mécanisme d’action
Le dispositif maintient un ensemble de micropipettes capables d’isoler des nanoparticules de petits volumes d’échantillons en appliquant un champ électrique considérablement faible sur toute la longueur des pipettes. L’architecture de la géométrie des pores a permis l’isolement de vésicules extracellulaires à partir de petits volumes d’échantillons de milieux de culture cellulaire conditionnés et de biofluides provenant de donneurs sains.
Dans ce travail, Sharma et son équipe ont isolé les biofluides des patients atteints de cancer, notamment le sérum, le plasma et l’urine, suivis d’une caractérisation multiparamétrique via la cytométrie en flux et le séquençage de miARN de nouvelle génération.
-
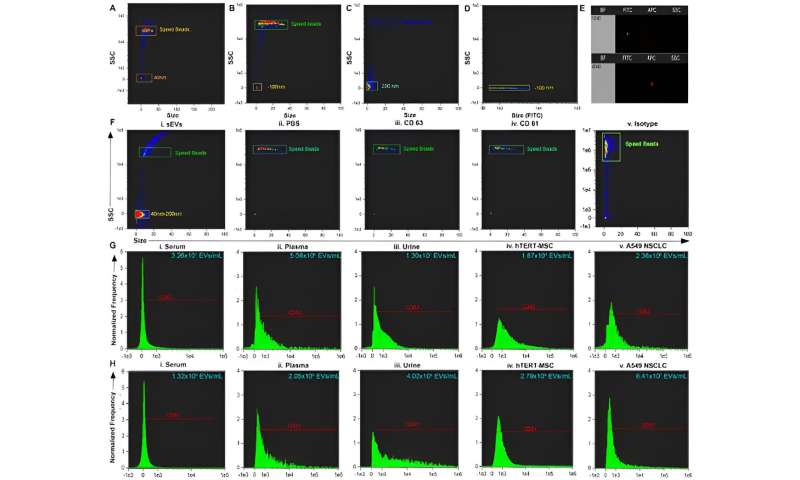
(A – C) Taille par rapport au SSC des billes et des billes de vitesse d’étalonnage. (D) Taille par rapport au FITC illustrant l’emplacement sur la diffusion latérale qui est positif pour les perles fluorescentes. (E) Diagramme de points représentatif de FITC par rapport à l’intensité de diffusion (en haut) et d’APC par rapport à l’intensité de diffusion (en bas). (F) Taille représentative par rapport au tracé SSC de i. petites vésicules extracellulaires (sEV) purifiées à partir de biofluides et de contrôles négatifs : ii. PBS iii. anticorps CD63 iv. anticorps CD81 et v. Isotype. (G) Histogramme représentatif des sEV CD63+ de i. sérum, ii. plasma, iii. urine et contrôles positifs : iv. sEV à cellules souches mésenchymateuses (CSM) immortalisées par hTERT et sEV dérivés du carcinome pulmonaire non à petites cellules (NSCLC) v. A549. (H) Histogramme représentatif des sEV CD81+ de i. sérum, ii. plasma, iii. urine et contrôles positifs iv. sEV MSC immortalisés par hTERT et sEV v. A549 NSCLC. Crédit: Rapports scientifiquesest ce que je: 10.1038/s41598-023-45409-4
-
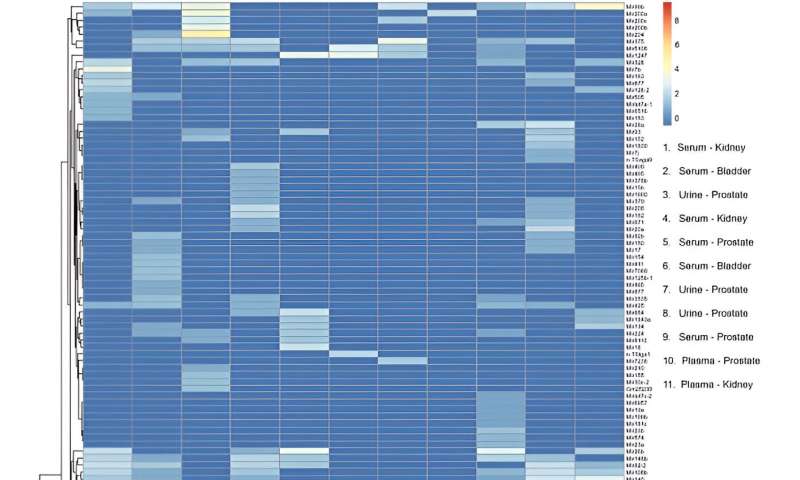
Carte thermique des transcrits de microARN isolés de petites vésicules extracellulaires (sEV) de sérum, de plasma et d’urine provenant de patients atteints de cancers des voies génito-urinaires. Les colonnes représentent des échantillons individuels. La légende indique le type de biofluide et le site du cancer pour chaque échantillon. Les lignes représentent les transcriptions des gènes microARN. L’échelle des barres de couleurs représente l’enrichissement des miARN. RStudio Desktop (version 2023.06.2 + 561, accessible sur a été utilisé pour la génération de cartes thermiques. Crédit : Rapports scientifiquesest ce que je: 10.1038/s41598-023-45409-4
L’équipe a purifié de petites vésicules extracellulaires à partir de sérum, de plasma et d’urine dans une solution saline tamponnée au phosphate en utilisant l’approche diélectrophorétique basée sur un isolant. Sharma et ses collègues ont utilisé la microscopie électronique à transmission pour confirmer la présence des vésicules et ont exploré l’analyse multiparamétrique de petites vésicules extracellulaires circulantes purifiées via la cytométrie en flux.
L’équipe a isolé les vésicules et les a analysées, suivies d’études conventionnelles de cytométrie en flux. Les chercheurs ont en outre montré la capacité et l’utilisation de l’appareil en caractérisant les isolats grâce au logiciel ImageStream.
Après le séquençage des miARN, l’équipe a cartographié 137 transcrits de miARN distincts et matures sur le génome humain à travers des échantillons afin d’inclure le dispositif dans les flux de travail d’analyse des biomarqueurs de miARN. Ils ont réalisé des profils transcriptomiques et effectué une analyse en composantes principales.
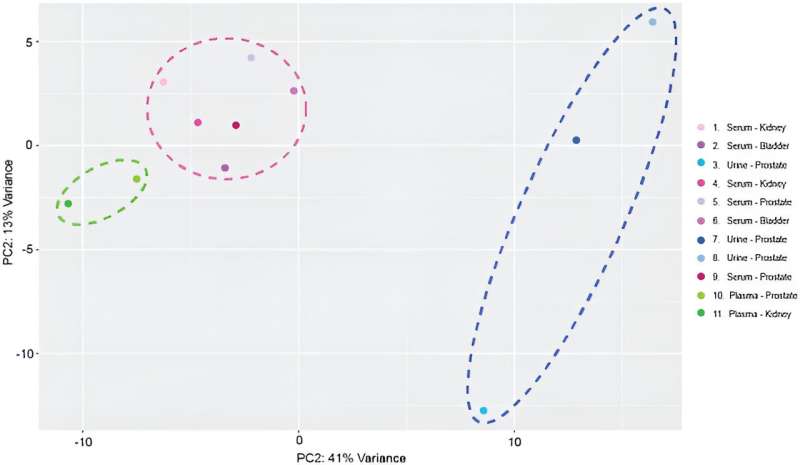
Analyse en composantes principales centrée à l’échelle des profils de miARN exosomal. Échantillons regroupés en fonction de l’origine exosomale. L’ovale pointillé vert met en évidence les échantillons extraits du plasma. Le cercle pointillé rose met en évidence les échantillons extraits du sérum. L’ovale pointillé bleu foncé met en évidence les échantillons extraits de l’urine. Crédit: Rapports scientifiquesest ce que je: 10.1038/s41598-023-45409-4
Perspectives
De cette manière, Manju Sharma et ses collègues ont montré la capacité et l’efficacité d’un dispositif diélectrophorétique basse tension et sans étiquette pour isoler de petites vésicules extracellulaires du sérum, du plasma et de l’urine de patients cancéreux grâce à la détection de particules submicroniques, et caractérisation multiparamétrique en utilisant des méthodes conventionnelles de cytométrie en flux et des méthodes avancées de cytométrie en flux.
Les concentrations d’ARN des travaux étaient comparables à celles des travaux antérieurs et confirmaient que la méthode d’isolement était une alternative viable à celles déjà établies en laboratoire. Les méthodes analytiques peuvent être utiles en tant que plates-formes de biopsie liquide pour isoler de petites vésicules extracellulaires et développer des plates-formes de diagnostic et de surveillance basées sur les vésicules extracellulaires.
Plus d’information:
Manju Sharma et al, Purification rapide et caractérisation multiparamétrique de petites vésicules extracellulaires circulantes à l’aide d’un dispositif de laboratoire sur puce sans étiquette, Rapports scientifiques (2023). DOI : 10.1038/s41598-023-45409-4
© 2023 Réseau Science X
Citation: Purification rapide et caractérisation de petites vésicules extracellulaires circulantes sur un laboratoire sur puce sans étiquette (15 novembre 2023) récupéré le 15 novembre 2023 sur
Ce document est soumis au droit d’auteur. En dehors de toute utilisation équitable à des fins d’étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.