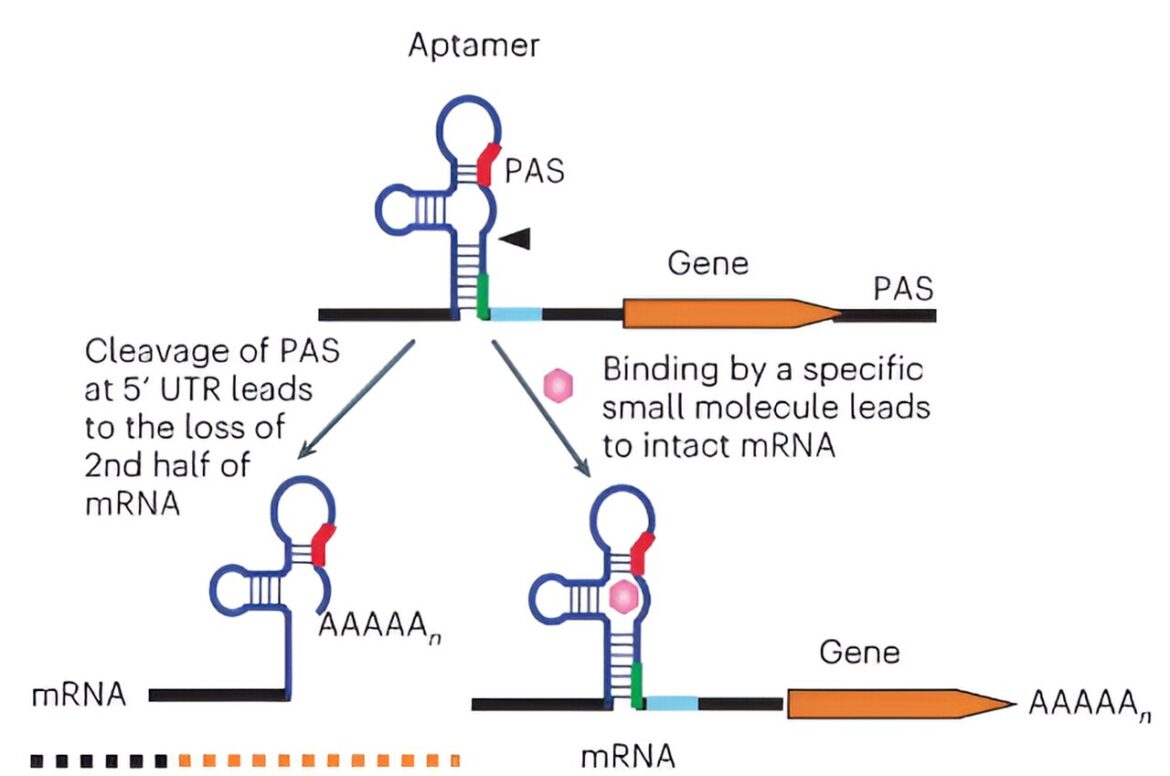
Un PAS synthétique (rouge) est inséré dans la 5′ UTR d’un transgène. Sans ligand, le clivage détruit la région codante de l’ARNm, perdant ainsi l’expression du transgène. La liaison du ligand à l'aptamère inhibe le clivage, entraînant la préservation de l'ARNm intact et, par conséquent, l'expression génique induite. Une région riche en GU (vert) et un motif MAZ riche en G (bleu) sont ajoutés pour augmenter la polyadénylation. Tous les motifs d’ARN modifiés agissent en cis. La pointe de flèche indique le site de clivage. Crédit: Biotechnologie naturelle (2024). DOI : 10.1038/s41587-023-01989-0
Tout comme un médecin ajuste la dose d'un médicament aux besoins du patient, l'expression des gènes thérapeutiques, ceux modifiés chez une personne pour traiter ou guérir une maladie par thérapie génique, doit également être maintenue dans une fenêtre thérapeutique. Il est important de rester dans la fenêtre thérapeutique, car une trop grande quantité de protéines pourrait être toxique et une quantité insuffisante pourrait entraîner un effet thérapeutique faible, voire inexistant.
Bien que le principe de la fenêtre thérapeutique soit connu depuis longtemps, il n’existe aucune stratégie pour le mettre en œuvre en toute sécurité, ce qui limite les applications potentielles de la thérapie génique en clinique.
Dans leur étude actuelle publiée dans la revue Biotechnologie naturelle, des chercheurs du Baylor College of Medicine font état d'une technologie permettant de réguler efficacement l'expression des gènes, une solution prometteuse pour combler cette lacune dans les applications cliniques de la thérapie génique. Un rapport de recherche sur cette avancée majeure a été publié dans le même numéro de revue.
“Bien qu'il existe plusieurs systèmes de régulation génétique utilisés dans les cellules de mammifères, aucun n'a été approuvé par la Food and Drug Administration des États-Unis pour des applications cliniques, principalement parce que ces systèmes utilisent une protéine régulatrice étrangère au corps humain, qui déclenche une réponse immunitaire contre “, a déclaré l'auteur correspondant, le Dr Laising Yen, professeur agrégé de pathologie et d'immunologie et de biologie moléculaire et cellulaire à Baylor.
“Cela signifie que les cellules qui expriment la protéine thérapeutique seraient attaquées, éliminées ou neutralisées par le système immunitaire du patient, rendant la thérapie inefficace.”
Depuis plus d’une décennie, Yen et ses collègues travaillent sur cette technologie et ont désormais trouvé une solution pour surmonter les principaux obstacles à son utilisation clinique. “La solution que nous avons trouvée n'implique pas de protéine régulatrice étrangère susceptible de provoquer une réponse immunitaire chez les patients. Au lieu de cela, nous utilisons de petites molécules pour interagir avec l'ARN, qui ne déclenchent généralement pas de réponse immunitaire”, a déclaré Yen.
“D'autres groupes ont également tenté de résoudre ce problème critique, mais les concentrations de médicaments qu'ils ont utilisées dépassent celles approuvées par la FDA pour les patients. Nous avons pu concevoir notre système de telle manière qu'il fonctionne à la dose approuvée par la FDA. “
Un interrupteur pour activer/désactiver les gènes au signal
Yen et ses collègues ont développé un système qui active les gènes à différents niveaux en utilisant de petites molécules à des doses approuvées par la FDA. Le commutateur est placé dans l’ARN, la copie du matériel génétique qui est traduite en protéine. Cette approche permet aux chercheurs de contrôler la production de la protéine en contrôlant son ARN.
L'ARN d'intérêt est d'abord conçu pour contenir un signal polyA supplémentaire, semblable à un « panneau d'arrêt » que les gènes utilisent naturellement pour marquer la fin d'un gène. Lorsque la machinerie cellulaire détecte un signal polyA dans l’ARN, elle effectue automatiquement une coupure et définit le point de coupure comme la fin de l’ARN. “Dans notre système, nous utilisons le signal polyA ajouté, non pas à la fin, mais au début de l'ARN, donc la coupure détruit l'ARN et donc la valeur par défaut n'est pas la production de protéines. Il est désactivé jusqu'à ce que nous l'activions avec la petite molécule”, a déclaré Yen.
Pour activer le gène au niveau souhaité, l’équipe a conçu un interrupteur sur l’ARN. Ils ont modifié une section de l'ARN proche du signal polyA de telle sorte qu'elle puisse désormais se lier à une petite molécule, la tétracycline approuvée par la FDA dans ce cas. “Lorsque la tétracycline se lie à cette section qui fonctionne comme un capteur sur l'ARN, elle masque le signal polyA et l'ARN sera désormais traduit en protéine”, a déclaré Yen.
Imaginez la situation future désormais possible. Un patient a reçu une thérapie génique qui fournit un gène pour compenser un gène défectueux à l’origine d’un problème de santé. Le gène reçu par le patient possède un commutateur qui permet au médecin de contrôler la production de la protéine thérapeutique.
Si le patient n’a besoin que d’une petite quantité de protéine thérapeutique, il ne prendra alors qu’une petite dose de tétracycline, ce qui n’activera que peu le gène thérapeutique. Si le patient a besoin de plus de protéines thérapeutiques, il prendra alors plus de tétracycline pour stimuler sa production. Pour arrêter la production de la protéine thérapeutique, le patient arrête de prendre de la tétracycline. En l’absence de tétracycline, l’interrupteur reviendra à sa position d’arrêt par défaut.
Certaines maladies peuvent bénéficier de la présence de faibles niveaux constants de protéines thérapeutiques. Dans ce cas, la technologie a la flexibilité de pré-ajuster le niveau par défaut aux niveaux spécifiés d’expression des protéines tout en conservant la possibilité d’augmenter l’expression avec la tétracycline.
“Cette stratégie nous permet d'être plus précis dans le contrôle de l'expression génique d'une protéine thérapeutique. Elle nous permet d'ajuster sa production en fonction des stades de la maladie ou de s'adapter aux besoins spécifiques des patients, le tout en utilisant la dose de tétracycline approuvée par la FDA.” » dit Yen. “Notre approche n'est pas spécifique à une maladie, elle peut théoriquement être utilisée pour réguler l'expression de n'importe quelle protéine et a potentiellement de nombreuses applications thérapeutiques.
“De plus, ce système est plus compact et plus facile à mettre en œuvre que les technologies existantes. Par conséquent, il peut également être très utile en laboratoire pour activer ou désactiver un gène d'intérêt afin d'étudier sa fonction.”
Plus d'information:
Liming Luo et al, Contrôle de l'expression des gènes des mammifères par modulation du clivage du signal polyA en 5 'UTR, Biotechnologie naturelle (2024). DOI : 10.1038/s41587-023-01989-0.
Un pas de plus vers une régulation sûre et efficace des gènes des mammifères, Biotechnologie naturelle (2024). DOI : 10.1038/s41587-023-02020-2
Fourni par le Baylor College of Medicine
Citation: Un nouveau commutateur active/désactive les gènes au bon moment, une étape prometteuse vers une thérapie génique plus sûre (2 janvier 2024) récupéré le 2 janvier 2024 de
Ce document est soumis au droit d'auteur. En dehors de toute utilisation équitable à des fins d'étude ou de recherche privée, aucune partie ne peut être reproduite sans autorisation écrite. Le contenu est fourni seulement pour information.